[Esta nota es una adaptación para público general de un artículo publicado en la revista Química Viva]
Esta es la historia de un hallazgo científico. Pero también es la historia de Joaquín, de 10 años, que sufre una enfermedad neurodegenerativa. Es la historia de sus padres, que se ocuparon de buscar con quiénes compartir la tristeza de transitar su condición hasta ese momento incurable. Es la historia de otras 400 familias en Argentina que se organizaron para rastrear qué se estaba haciendo en los laboratorios del mundo en busca de una esperanza, pero que se toparon también con la especulación de una industria poderosa. Es la historia de un grupo de científicos de nuestro país que un día como cualquier otro se encontraron con un pedido de lo más inusual, con interlocutores inesperados, con un trayecto que pese a su larga experiencia les resultaba nuevo. Y en el que, al menos por el momento, ya pudieron encontrar algunas satisfacciones.
A principios de Junio tuvimos un gran anuncio protagonizado por el laboratorio del biólogo Alberto Kornblihtt. Este grupo del Instituto de Fisiología, Biología Molecular y Neurociencias (IFIBYNE) dependiente de UBA y CONICET salió en los medios del país por haber dado un paso en la lucha contra una elusiva enfermedad. Pero el caso no es solamente interesante por su costado científico, sino porque ilustra la organización de familiares de pacientes y sus diálogos con investigadores e instituciones: fue el grupo que nuclea a 400 familias de personas afectadas por esta patología quien puso en marcha los engranajes del anunciado avance contra la Atrofia Muscular Espinal (AME).
¿Qué es la AME?
La enfermedad neurológica que motivó esta investigación es en muchos casos ciertamente devastadora: causa en las personas afectadas una debilidad muscular progresiva que en muchos casos puede llegar a ser terrible. En la forma más común y grave, bautizada AME1, los primeros síntomas aparecen dentro de los seis meses de vida y sin intervención suele ser letal antes de los dos años. Su severidad y la rapidez de su avance depende de factores genéticos, y el otro extremo del espectro incluye formas de comienzo adulto que no afectan la expectativa de vida, aunque sí su calidad.
Años de investigación sirvieron para identificar a las culpables: son mutaciones en el gen SMN1 (por Survival Motor Neuron 1) que afectan su funcionamiento. Ese nombre (en español, "supervivencia de neuronas motoras") no fue puesto caprichosamente: la proteína SMN que se fabrica gracias a este gen (cuando no está afectado) es vital para que las neuronas se mantengan vivas. Cuando pierde su función las neuronas comienzan a morir, con los efectos incapacitantes que ya mencionamos. Hasta hace unos años no existían tratamientos, y fueron necesarios muchos trabajos en ciencia básica y estudios específicos sobre los mecanismos de la enfermedad para que en 2017 finalmente se aprobase el nusinersen, una droga desarrollada de forma específica para la AME.
¿Las ventajas de este tratamiento? Incluso en los casos más graves su aplicación rápida puede hacer una diferencia abismal. Vanina Sánchez, presidenta de Familias AME Argentina (FAME), lo ilustra claramente: cuando son diagnosticados y tratados muy tempranamente hasta los pacientes del tipo más severo pueden desarrollarse de forma normal. En una familia con dos hermanitos afectados por la misma mutación, uno de ellos depende de un respirador y una sonda gástrica. Su hermano menor, al que lograron diagnosticar y tratar desde recién nacido, puede ir a la plaza y usar el tobogán como cualquier niño no afectado.
Por otro lado, la versión comercial del tratamiento, llamada Spinraza, estuvo desde su desarrollo en el ojo de la tormenta por ser una de las medicinas más caras del mundo. Aunque fue un producto originalmente desarrollado con fondos públicos, muy pronto un laboratorio financió los ensayos clínicos restantes y se hizo con los derechos de la droga. Su aplicación consta de cuatro dosis iniciales por un total 750.000 dólares, y a partir de ese momento, anualmente se aplican tres inyecciones que cuestan otros 375.000. Algo que ninguna familia puede pagar, y que para los pacientes más graves significa la diferencia entre la vida y la muerte. En Argentina hubo una larga pulseada entre el Estado y el laboratorio que comercializa la droga, Biogen, para negociar el acceso. Luego de un primer pacto muy desventajoso para nuestro país, que permitía a la empresa especular con el precio y mantenerlo en la confidencialidad, se firmó en 2021 un nuevo convenio. Este acuerdo asegura que las prepagas, obras sociales o el Estado cubran la totalidad del medicamento para los casos de AME1. A su vez el laboratorio ha aceptado bajar el costo, que igualmente, sigue siendo exorbitante: unos 80.000 dólares por dosis. Con tres inyecciones al año eso significaría casi un cuarto de millón de dólares anual por cada paciente.

Con o sin convenios, adquirir drogas para tratar la AME puede ser prohibitivo para un país periférico. Incluso en el norte global el acceso para los pacientes puede depender de las vicisitudes de los sistemas de salud y de los nexos, no siempre transparentes, entre el laboratorio, los seguros médicos y los Estados. Además su costo restringe en muchos casos la cobertura sólo a los casos más graves. Esta fue una de las preocupaciones que motivó el estudio que fuese anunciado por el laboratorio del IFIBYNE: ¿puede mejorarse la eficiencia del fármaco para hacerlo más accesible a quienes lo necesiten?
Luces y sombras de un genoma inquieto
Para entender cómo funciona el nusinersen y cómo el equipo de Alberto Kornblihtt está contribuyendo a mejorar el tratamiento hay que adentrarse un poco en nuestra historia evolutiva reciente. La región del ADN en que se encuentra el ya mencionado gen SMN1 es testigo del dinamismo de nuestro material genético. Se trata de una zona que en el pasado de la especie humana sufrió cambios y hoy contiene secuencias que se parecen mucho entre sí, pero están invertidas. Estas regiones pueden “pegotearse” con cierta facilidad cuando se copia el ADN, y es relativamente frecuente que se pierdan o alteren fragmentos que incluyen al gen SMN1. Si eso ocurre en la generación de óvulos o espermatozoides, se puede heredar esta versión mutada del gen que causa la AME. Semejante inestabilidad explica que ésta sea la más común de las enfermedades genéticas que resultan en muerte infantil.
Tal vez paradójicamente, esta agitada historia de nuestro genoma fue la llave para el desarrollo del nusinersen. Dijimos que esta región tiene partes del ADN que están repetidas, y eso significa que existe una “versión alternativa” de SMN1 llamado SMN2, una réplica casi exacta. “Casi” es la palabra clave: aún siendo escasas, las diferencias entre SMN1 y SMN2 impiden que el duplicado compense las falencias en el gen original. La principal causa es una mutación en lo que se llama un “sitio de splicing” de SMN2.
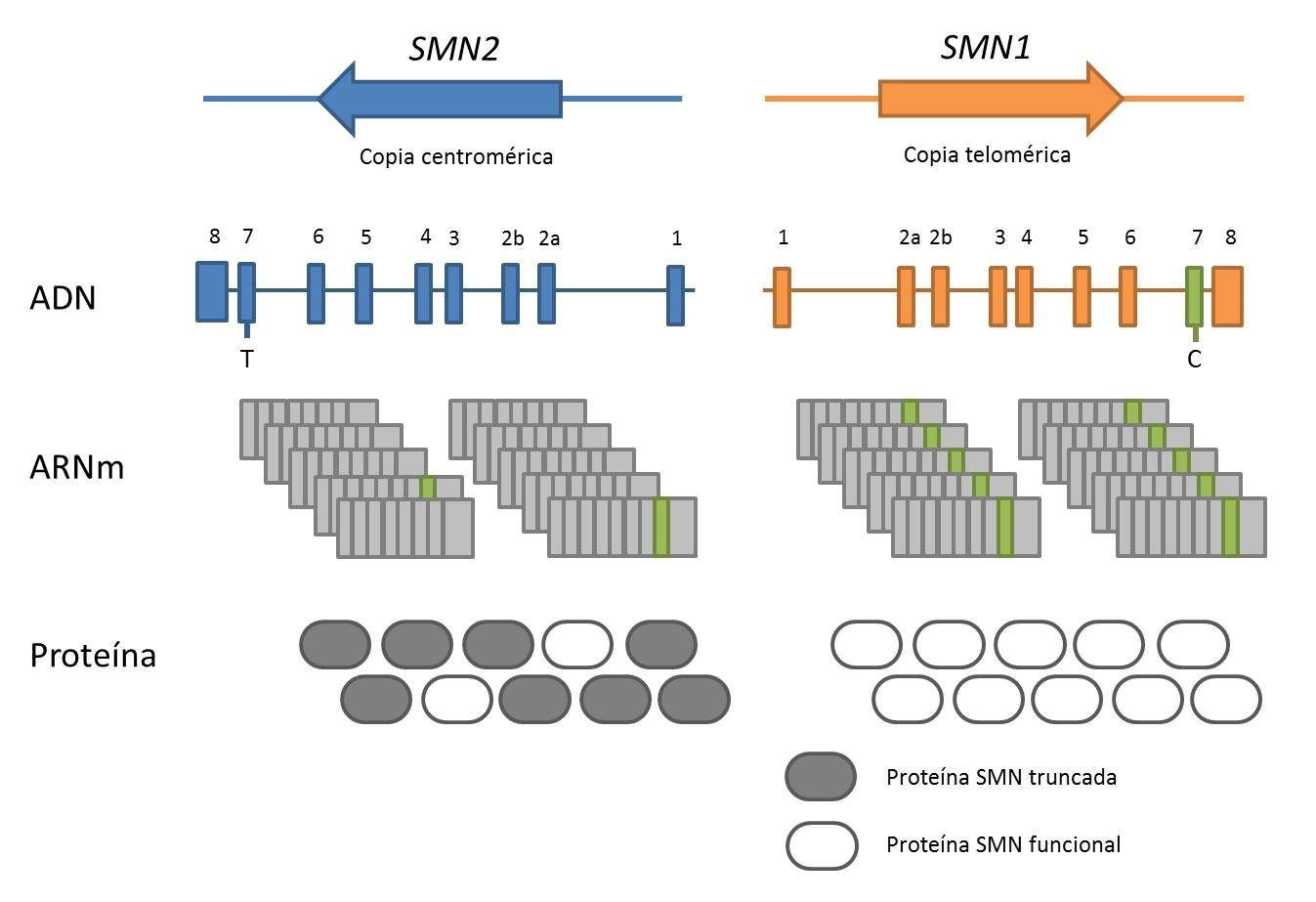
¿Qué es el splicing? Cuando en las células se “lee” un gen que se encuentra en el ADN, primero se copia como molécula de ARN llamado “mensajero”, del que se “decodificará” una proteína. El ARN mensajero no queda como una copia exacta del ADN original, sino que es procesado, y algunas partes de su secuencia se cortan y se eliminan. Pero no siempre: en muchos casos, este proceso que llamamos “splicing” puede ocurrir o no, dependiendo del contexto, y significa que se pueden obtener varias proteínas alternativas de un mismo gen en distintas proporciones, dependiendo de muchos factores. Kornblihtt describe este fenómeno de “splicing alternativo” como una especie de “sastre molecular” que en base a telas exactamente iguales, en diferentes condiciones puede cortar y pegar en distintos lugares para confeccionar diversos vestidos. Pero… ¿qué tiene que ver este proceso con la AME?
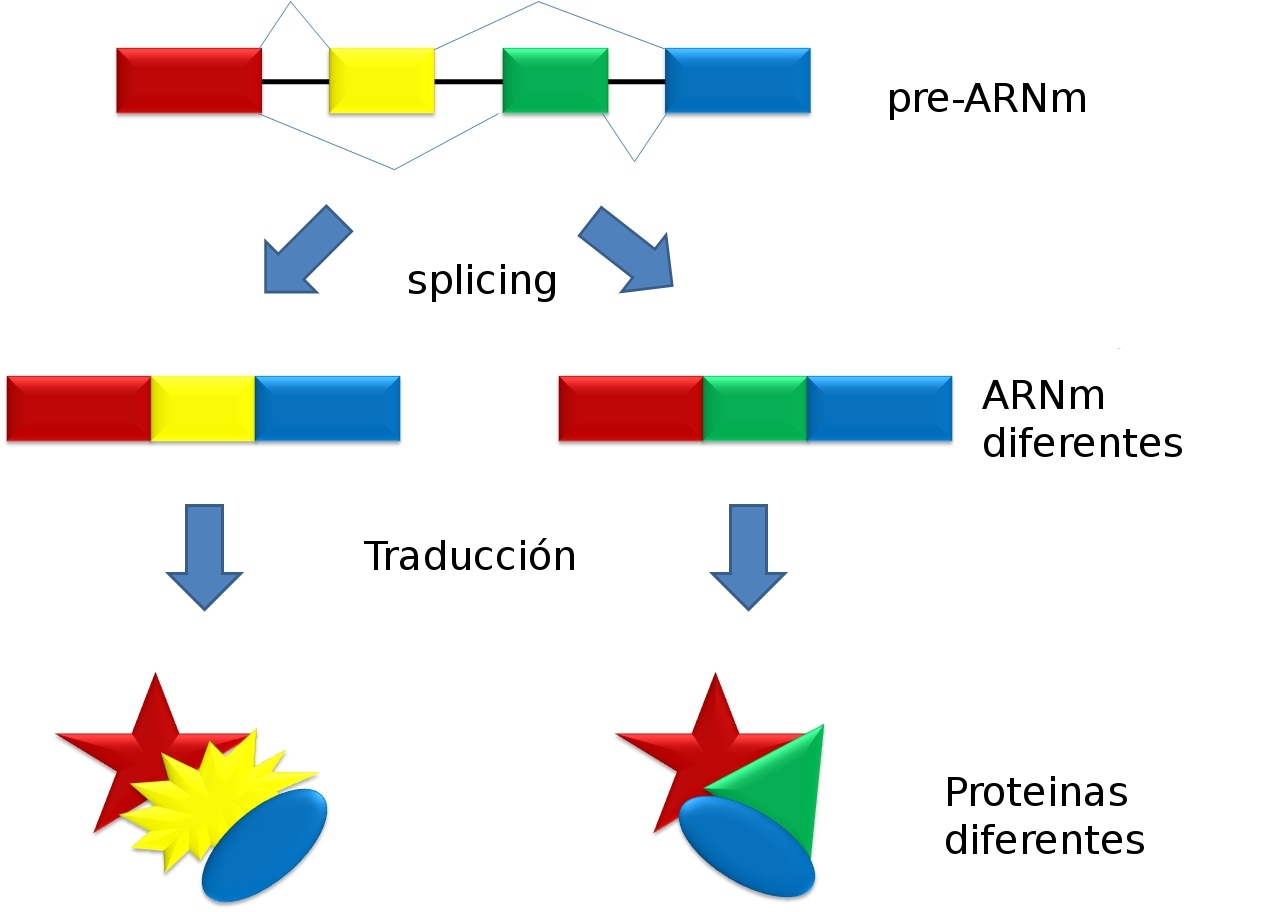
Dijimos que el gen SMN2 era casi igual al gen mutado SMN1, excepto por algunos cambios, uno de ellos en un sitio de splicing. Por ese cambio, al procesarse el ARN de SMN2, a diferencia de lo que ocurre en SMN1 en personas sanas, una parte importante del gen (que llamaremos “exón 7”) se elimina en una alta proporción de los mensajeros. La proteína SMN que se genera es normal pero gran proporción de las moléculas producidas son muy inestables, y las células las degradan antes de que puedan actuar. Por eso es que SMN2 no alcanza para compensar las alteraciones en SMN1 en personas afectadas. Aún teniendo este “backup” genético, la proteína que produce no llega a salvar a las neuronas de los pacientes.
Si tan solo se pudiese modificar el equilibrio del splicing alternativo de SMN2 para retener ese exón 7, aumentaría la cantidad de la proteína SMN estable y funcional. Y de hecho gran parte de los esfuerzos contra la AME se enfocan en este proceso y logran enlentecer el curso de la enfermedad. Así funciona el nusinersen, un compuesto que desarrolló el uruguayo Adrián Krainer en su laboratorio en Cold Spring Harbor. Es un “oligonucleótido antisentido”, es decir una secuencia corta de ARN que se inyecta directamente en el líquido cefalorraquídeo de los pacientes. Esta molécula puede pegarse al ARN mensajero de SMN2 en un sitio específico, logrando inhibir el splicing que elimina al exón 7. De esta forma, la droga aumenta la cantidad de proteína SMN estable y funcional capaz de “rescatar” a las neuronas motoras. Esta fue la primera droga disponible contra la AME.
Ciencia básica, ciencia aplicada y ciudadanos científicos
La historia no termina aquí, por supuesto. Hay muchos factores que pueden afectar los procesos de splicing, por lo que la eficacia del nusinersen es variable y mejorable. Aquí radica el potencial para bajar el costo del tratamiento: lograr que el fármaco funcione de forma más efectiva y en menores cantidades encontrando otros factores que inclinen la balanza a favor de la inclusión del exón 7. Esta era una de las esperanzas de Kornblihtt y sus colaboradores, con una ya amplísima historia de investigación de los mecanismos del splicing alternativo, cuando empezaron a trabajar en este desarrollo.
Pero aún con su gran experiencia en el tema, igual este fue el comienzo de un nuevo camino para el laboratorio del biólogo. “Nosotros siempre trabajamos en los mecanismos básicos, en ciencia básica – aclaró Kornblihtt en una conferencia de prensa difundida por CONICET – pero hace unos seis años golpearon la puerta de mi oficina los padres de los niños que sufren AME”. A sabiendas de que el principal tratamiento para la enfermedad involucraba cambiar el equilibrio en el splicing alternativo, fueron ellos quienes se pusieron al hombro la tarea de contactar a los expertos. En Argentina, Kornblihtt era “número puesto”.
La colaboración no empezó de forma inmediata: como manifestó el investigador en su charla, la relación entre los científicos y los pacientes o sus familias puede ser complicada. Siempre existe el riesgo de que las expectativas no se cumplan, y sobre todo ante una patología tan cruel, es posible alimentar involuntariamente esperanzas desmedidas. Las familias insistieron. “Desde 2003 teníamos un sueño, que era que en algún momento se investigue en nuestro país” contó emocionada Vanina Sánchez en el evento. “Alberto nos cerró una puerta pero dejó abierta una ventana. Se quedó pensando, un tiempo después nos llamó y nos dijo que sí”. Como aclaró el biólogo, los familiares no sólo querían que se hiciera investigación básica en el país, sino tener contactos científicos que les permitieran interpretar los avances que se producían en laboratorios del exterior. Así fue que estos ciudadanos, originalmente agrupados para contenerse mutuamente ante la devastadora y hasta ese momento intratable enfermedad, se involucraron de forma directa en la investigación. No sólo financiaron parte de los reactivos hasta que el laboratorio acumuló suficiente evidencia para acceder a los subsidios necesarios, sino que establecieron también un ida y vuelta invitando a los investigadores argentinos a comunicar sus descubrimientos en reuniones en el país y el mundo.
Aprovechando la sinergia
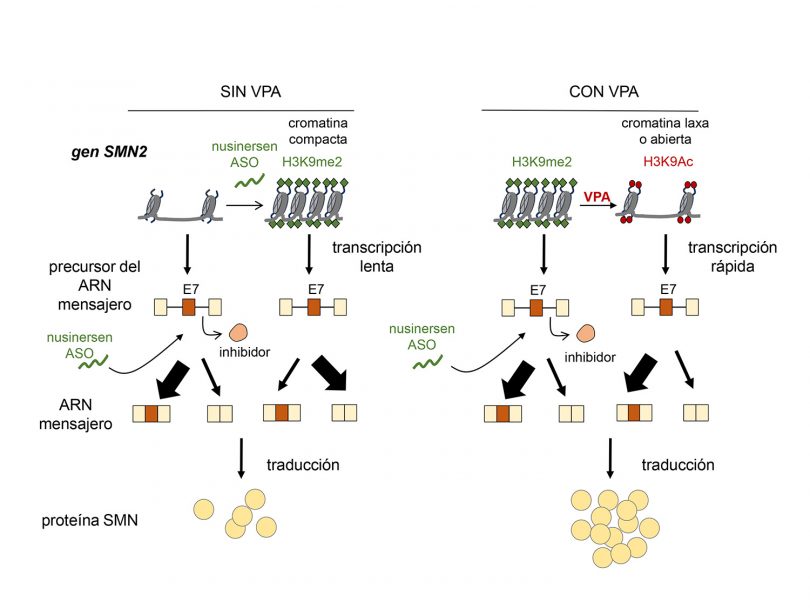
En el laboratorio del IFIBYNE ya habían detectado que el splicing alternativo suele depender del grado de condensación del ADN, es decir, si nuestro material genético está muy densamente “empaquetado” o más bien relajado, como una lana que recién terminamos de desovillar. Esta estructura es dinámica y depende mucho de los complejos que forman el ADN con proteínas, una dupla que conocemos como “cromatina”. Se sabe que cuando la cromatina se encuentra más laxa, los genes se “leen” a mayor velocidad. Luciano Marasco, becario doctoral y primer autor del paper, explica en el video difundido por CONICET por qué el grupo puso su atención en este fenómeno: en el caso particular de SMN2, una relajación de la cromatina en esa zona podría ser clave para evitar este tan inconveniente splicing y así mejorar el tratamiento. De hecho, verificaron que el nusinersen tiende a compactarla, por lo que limita su propia efectividad. Contrarrestar este efecto indeseado del fármaco podría mejorar su funcionamiento. Esa fue la punta del hilo del que empezaron a tirar.
Para eso tuvieron que probar con los compuestos ya conocidos por su efecto en la condensación del ADN. Así llegaron al ácido valproico, un medicamento usado en algunos casos de epilepsia y trastorno bipolar que ejerce sus efectos relajando la estructura de la cromatina. La apuesta era por una terapia combinada con el nusinersen, en la que se potenciasen los efectos de ambas drogas para evitar el splicing del exón 7 en SMN2. Y, al menos en modelos animales, funcionó, como anunciaron en la conferencia de prensa y en un paper publicado en Junio en la revista Cell.
Con Marasco como primer autor, el trabajo presenta los resultados en ratones: vieron efectos positivos al administrar una combinación de nusinersen y ácido valproico, tanto en el splicing de SMN2 como en el nivel de proteína estable que se producía. Además la terapia “rescataba” a los animales a nivel neuronal, en el crecimiento y la supervivencia. Aunque son buenas noticias, todavía resta conocer los efectos de la combinación en pacientes de AME. Vanina Sánchez se ocupó de aclarar en la conferencia de prensa que la expectativa entre las familias es muy grande, pero que tienen cautela y se encuentran a la espera de los ensayos clínicos que corroboren si la terapia combinada es efectiva en humanos.

Por lo pronto, todos los participantes de la conferencia aprovecharon para destacar que tanto el desarrollo original del nusinersen como de esta terapia combinada hubiesen sido imposibles si no fuese por la inversión en ciencia básica, y mencionaron la importancia de la soberanía científica y del rol del Estado para implementar políticas de largo plazo independientes de las necesidades del mercado. Vale destacar que al menos hasta esta etapa el financiamiento de los ensayos de la terapia combinada ha provenido de las organizaciones de familias, fundaciones o de fondos públicos, sin el involucramiento de multinacionales farmacéuticas que eventualmente pudiesen especular con el costo y llenar sus bolsillos aprovechando una terapia desarrollada originalmente con fondos públicos.
